研究发现调控体细胞重编程的“变阻器”分子。 近日,中国科学院广州生物医药与健康研究院跨物种干细胞与疾病建模研究组首次发现,转录因子可充当调节细胞命运转变的变阻器而非简单开关,并揭示了核受体在细胞命运塑造中的独特调控作用。相关成果在线发表于《干细胞报告》(Stem Cell Reports),同期配发了美国伊利诺伊大学芝加哥分校教授Constantinos Chronis撰写的专题预览。
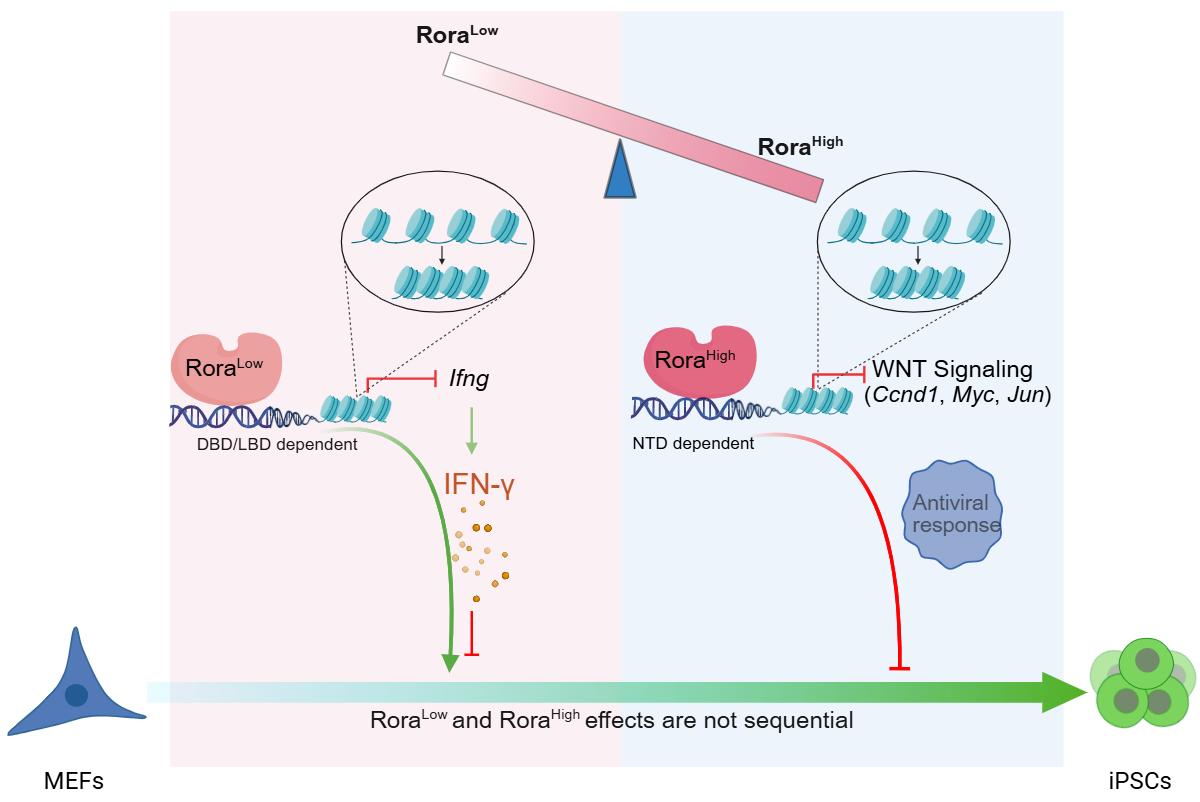 RORA在体细胞重编程中的低剂量促进、高剂量抑制效应模型。研究团队供图
RORA在体细胞重编程中的低剂量促进、高剂量抑制效应模型。研究团队供图
论文通讯作者、中国科学院广州生物医药与健康研究院研究员刘晶指出,该研究以诱导多能干细胞为模型,对小鼠核受体家族蛋白进行了系统性的重编程活性筛选。结果发现,视黄酸相关孤儿受体α(RORA)以剂量依赖的方式调节体细胞重编程:低剂量下,RORA与炎症信号(IFN-γ通路)降低相关,促进重编程;高剂量下,RORA与WNT信号输出降低相关,抑制重编程。
核受体作为一类整合多种细胞信号的重要转录因子,在发育、代谢、免疫等过程中发挥关键作用,但其在体细胞重编程中的功能和机制尚不明确。
在国家重点研发计划、国家自然科学基金等项目资助下,研究团队对小鼠49个核受体蛋白进行系统性重编程活性测试后,首先发现ROR亚家族成员(Rora、Rorb、Rorc)均能一致性地提升重编程效率,其中Rora的促进效果最为显著。进一步的剂量梯度实验意外发现:随着Rora表达量升高,重编程效率呈现先升后降的变化,表现出清晰的低剂量促进、高剂量抑制效应。
研究团队进一步开展了Rora的结构与功能研究。通过结构域拆分,发现DNA结合结构域与配体结合结构域是Rora发挥促进功能所必需,而N端结构域则是介导高剂量抑制效应的关键区域。在机制层面,研究团队整合RNA-seq、CUTTag、ATAC-seq、IP-MS等多组学数据,提出如下模型:低剂量下,Rora通过削弱IFN-γ相关的免疫信号来促进重编程;高剂量下,Rora则通过抑制WNT通路输出导致重编程效率下降。该模型为理解Rora的剂量依赖性双重效应提供了机制线索。
该研究提出了转录因子作为细胞命运转变的变阻器而非简单开关的观点,拓展了人们对细胞命运调控的认知。研究结果揭示了核受体剂量调节参与细胞命运转变的新范式,为细胞命运的精细调控及工程化改造提供了新思路。(来源:中国科学报 朱汉斌)
相关论文信息:https://doi.org/10.1016/j.stemcr.2026.102870
作者:刘晶等 来源:《干细胞报告》

