科研人员利用可见光催化破解蛋白质标记选择性瓶颈。近日,中国科学院上海有机化学研究所研究团队等,在生物正交标记技术领域取得进展。研究团队发展出可见光驱动的酮基自由基偶联新策略,在活细胞层面实现了蛋白质的原子级精度标记与交联。该方法通过可见光催化,高效生成稳定的二芳基酮自由基,有效规避了传统紫外激发技术因高能光照导致的选择性差、副反应多、背景干扰强等固有缺陷,提升了标记特异性与生物相容性。
研究团队系统解析了传统紫外激发交联技术的核心瓶颈,即其产生的高活性且难以调控的反应中间体三线态双自由基,易引发环加成和氢原子攫取等副反应,导致非特异性交联和生物分子损伤。同时,团队构建了新型可见光催化体系。该体系可在中性水溶液中高效生成稳定的二芳基酮自由基,实现了生物正交条件下的精准频哪醇偶联。这一策略将副反应发生率从传统方法的20%以上降至5%以下,提升了蛋白质交联的特异性与生物相容性。
这一技术仅需在目标蛋白单一位点嵌入光交联探针苯甲酮丙氨酸,即可通过光催化高效触发交联反应,实现高效精准的蛋白质交联,明显优于传统的多步骤、低特异性交联方法。同时,在PyrI4同源二聚体及Trx/PAPS异源复合物研究中,该策略均展现出高度特异性交联,且工程化蛋白保持了天然结合亲和力。研究团队通过高精度串联质谱分析,直接鉴定出频哪醇型交联键的形成,并在原子尺度上解析了蛋白质相互作用界面。
该研究为解析活细胞内蛋白质动态互作与功能提供了高精度、低扰动的新一代化学工具。
相关研究成果发表在《美国化学会志》上。研究工作得到国家自然科学基金委员会、中国科学院、上海市的支持。
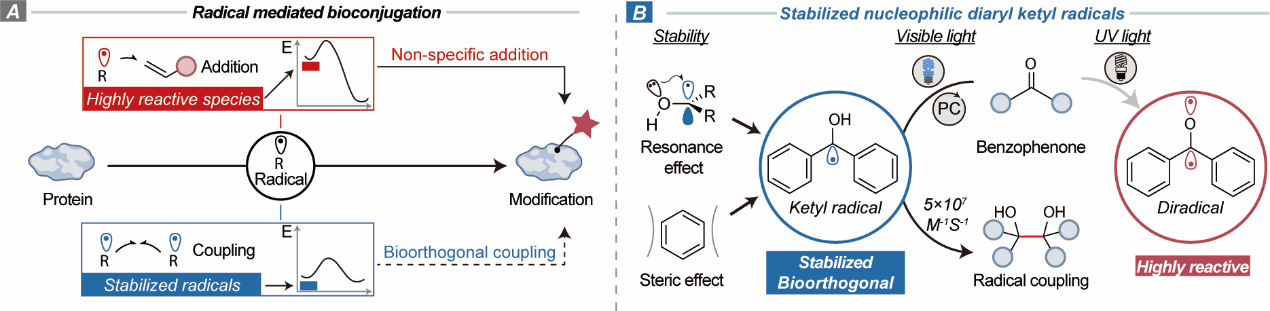
从非特异性副反应(左)到精准自由基偶联(右)
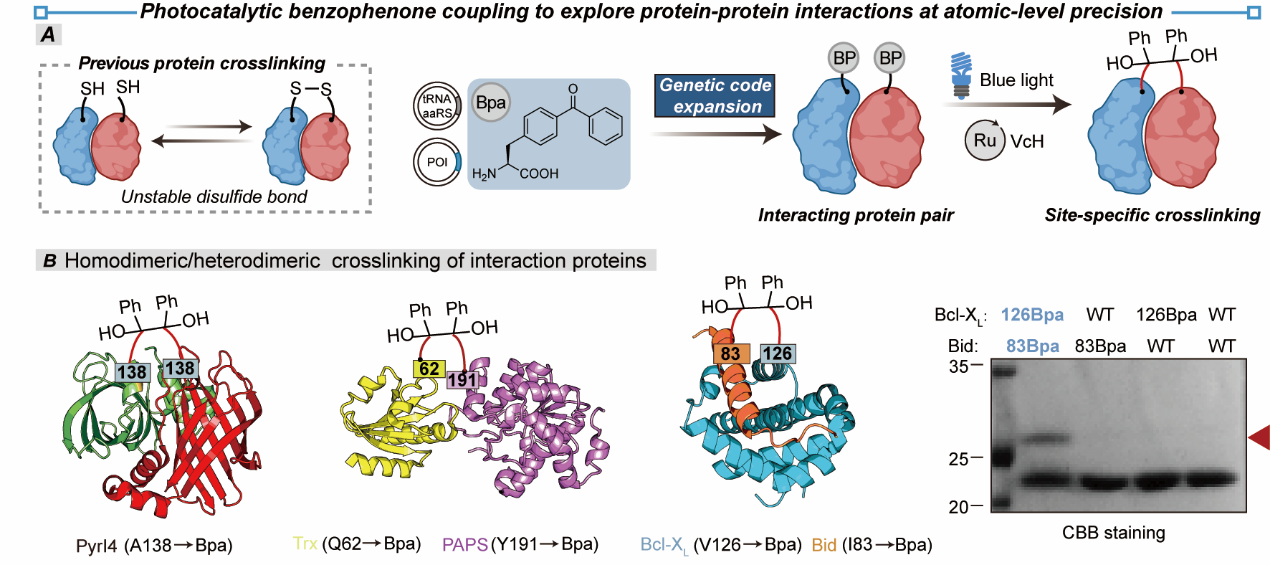
频哪醇键实现原子精度蛋白质交联
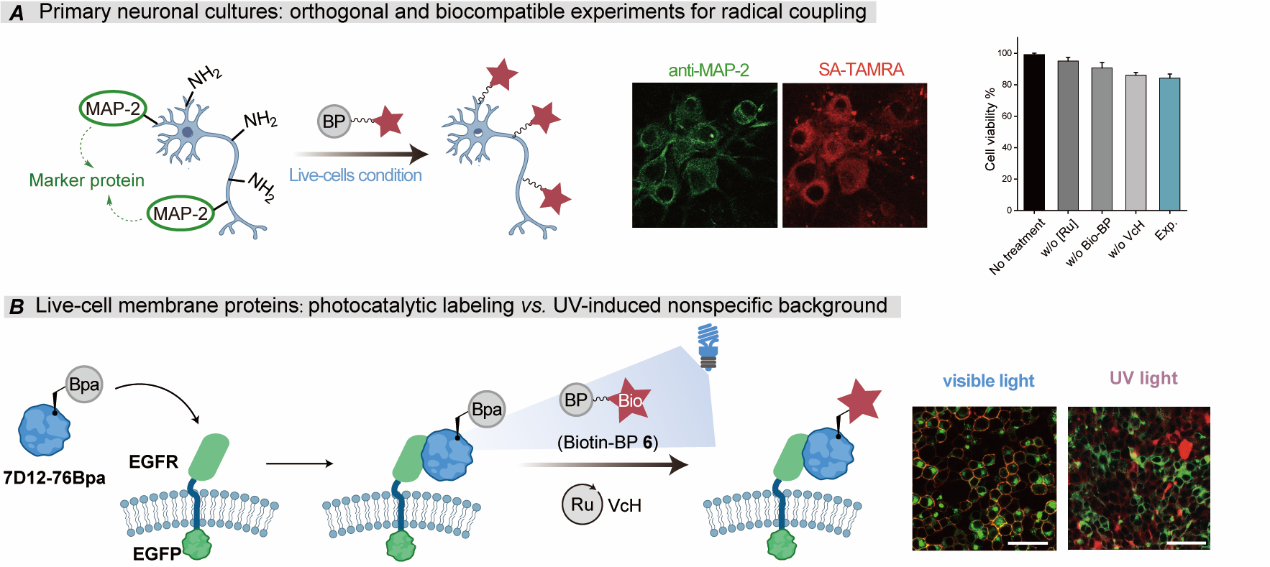
原代神经元及癌细胞靶向标记技术的新突破
研究团队单位:上海有机化学研究所

